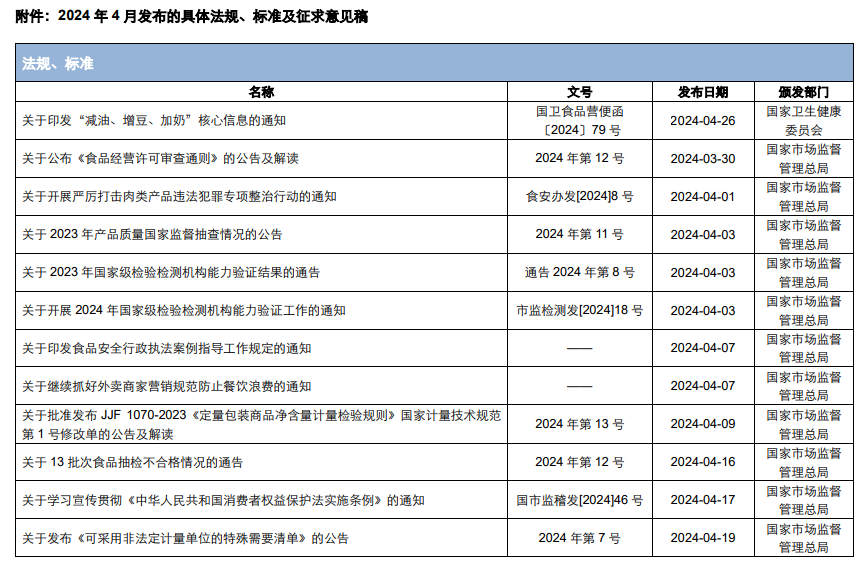
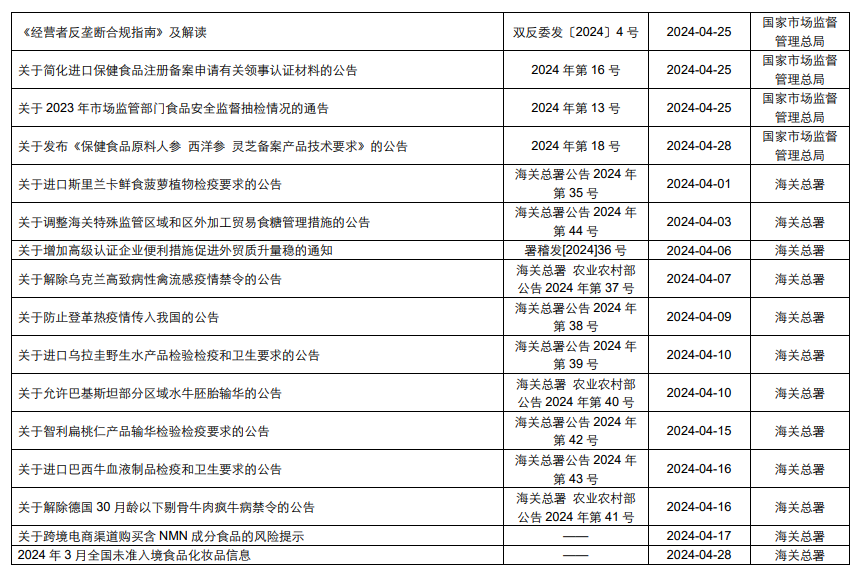
本月,各政府監管機構陸續發布了一些(xiē)食品相關的重要法規标準、征求意見稿及公告。其中,國務院發布《關于開(kāi)展嚴厲打擊肉類産品違法犯罪專項整治行(xíng)動的通(tōng)知》;國家(jiā)市場(chǎng)監督管理(lǐ)總局發布《食品經營許可(kě)審查通(tōng)則》、關于公開(kāi)征求《食品添加劑生(shēng)産許可(kě)審查細則(征求意見稿)》意見的通(tōng)知、關于批準發布JJF 1070-2023《定量包裝商品淨含量計(jì)量檢驗規則》國家(jiā)計(jì)量技(jì)術(shù)規範第1号修改單的公告及解讀、關于發布《保健食品原料人(rén)參 西洋參 靈芝備案産品技(jì)術(shù)要求》的公告;海關總署發布《關于跨境電(diàn)商渠道(dào)購買含NMN成分食品的風險提示》的公告;國家(jiā)食品安全風險評估中心對拟微球藻油等3種新食品原料公開(kāi)征求意見。
為(wèi)了更好地幫助企業落地法規,中食安信對2024年4月份發布的重點法規、标準以及征求意見稿進行(xíng)了簡單解讀,同時(shí)對本月發布的食品相關法規、标準等進行(xíng)了彙總,供大(dà)家(jiā)參考。
01
《食品經營許可(kě)審查通(tōng)則》發布、《食品添加劑生(shēng)産許可(kě)審查細則》公開(kāi)征求意見
以2023年12月修訂實施的《食品經營許可(kě)和(hé)備案管理(lǐ)辦法》為(wèi)基礎,在嚴格重點領域許可(kě)審查要求、簡化食品經營許可(kě)程序、增加新興業态許可(kě)審查等方面進行(xíng)修訂,比如:針對“拍黃瓜”“泡茶”等簡單制(zhì)售食品安全風險較低(dī)食品的,明(míng)确可(kě)以在保障食品安全的前提下适當簡化設施設備、專門(mén)區(qū)域等審查內(nèi)容,并在食品經營許可(kě)證副本中标注簡單制(zhì)售,明(míng)确設置專間(jiān)或專用操作(zuò)區(qū)的具體(tǐ)情形,充分釋放改革紅利,營造便民利企營商環境。
自2015年新修訂的食品安全法頒布實施後,食品添加劑生(shēng)産許可(kě)與食品生(shēng)産許可(kě)合并,2010版的《食品添加劑生(shēng)産許可(kě)審查通(tōng)則》作(zuò)廢,随後《食品生(shēng)産許可(kě)審查通(tōng)則》先後發布了2016版和(hé)2022版,作(zuò)為(wèi)食品和(hé)食品添加劑生(shēng)産許可(kě)審查共用的通(tōng)則。去年公安部嚴厲打擊“兩超一非”食品領域犯罪,多(duō)涉及食品生(shēng)産環節超範圍超限量使用食品添加劑,為(wèi)強化此問題系統治理(lǐ),結合食品添加劑行(xíng)業特征和(hé)監管需要制(zhì)定《食品添加劑生(shēng)産許可(kě)審查細則》,來(lái)細化生(shēng)産許可(kě)審查要求,重點包括:明(míng)确複配食品添加劑和(hé)食品用香精配方和(hé)命名要求、防控食品用色素副染料超标風險以及針對标簽和(hé)說明(míng)書(shū)标示不規範問題,明(míng)确食品添加劑标簽和(hé)說明(míng)書(shū)具體(tǐ)審查要求,強調食品添加劑使用範圍應在規定的食品類别範圍內(nèi)選擇标注、用量應不高(gāo)于規定的最大(dà)使用量。
02
《保健食品原料人(rén)參 西洋參 靈芝備案産品技(jì)術(shù)要求》發布
2023年12月,市場(chǎng)監管總局發布《保健食品原料目錄 人(rén)參、西洋參、靈芝》,将人(rén)參、西洋參、靈芝納入保健食品原料目錄。2024年4月30日,市場(chǎng)監管總局發布《保健食品原料人(rén)參 西洋參 靈芝備案産品技(jì)術(shù)要求》,自2024年5月1日起對以人(rén)參、西洋參、靈芝為(wèi)原料的保健食品實施備案管理(lǐ)。
這也是首次将我國傳統中藥類原料的保健食品納入備案管理(lǐ),故特别強調備案産品應符合傳統食用方式、傳統食用人(rén)群和(hé)傳統加工工藝。同時(shí)要求備案人(rén)必須具備自己加工保健食品的能力,暫不具備生(shēng)産條件的,不納入備案管理(lǐ)。在傳承傳統保健養生(shēng)文化的同時(shí),保障備案産品的安全性和(hé)有(yǒu)效性。
03
拟微球藻油等3種新食品原料公開(kāi)征求意見
2024年4月28日,新食品原料拟微球藻油、蛋黃磷脂蛋白公開(kāi)征求意見,主要內(nèi)容為(wèi):拟微球藻油推薦食用量≤2克/天,嬰幼兒、孕婦和(hé)哺乳期女不宜食用,标簽、說明(míng)書(shū)應當标注不适宜人(rén)群和(hé)食用限量;蛋黃磷脂蛋白推薦食用量≤5克/天,使用範圍不包括嬰幼兒食品,标簽、說明(míng)書(shū)應當标注食用限量。此外,黑(hēi)麥花(huā)粉經國家(jiā)衛生(shēng)健康委2023年第3号公告批準為(wèi)新食品原料,基于行(xíng)業數(shù)據,通(tōng)過專家(jiā)評審委員會(huì)審查,現拟将公告中膳食纖維的含量要求修訂為(wèi)≥30%,反饋截止日期為(wèi)2024年5月28日。
04
JJF 1070-2023《定量包裝商品淨含量計(jì)量檢驗規則》國家(jiā)計(jì)量技(jì)術(shù)規範第1号修改單
《定量包裝商品淨含量計(jì)量檢驗規則》(JJF 1070-2023)在本月發布了第1号修改單,并将其延期至2024年10月12日正式實施實施。公告中修訂了兩點內(nèi)容:
1.修改對淨含量标注的構成要求,來(lái)引導企業為(wèi)消費者提供更為(wèi)清晰的淨含量信息,例如:某企業生(shēng)産的食用油,淨含量标注為(wèi)5.436 L,若将其标注改為(wèi)不超過三位有(yǒu)效數(shù)字,如:5.5 L,則能讓消費者更簡潔、清晰地理(lǐ)解該商品淨含量。
2. 将“淨含量标注應以清晰可(kě)見的粗體(tǐ)字體(tǐ)标注”修改為(wèi):“淨含量标注應清晰可(kě)見”,便于要求企業為(wèi)消費者提供更為(wèi)清晰、準确的淨含量信息。
05
關于跨境電(diàn)商渠道(dào)購買含NMN成分食品的風險提示
今年4月,海關總署發布《關于跨境電(diàn)商渠道(dào)購買含NMN成分食品的風險提示》,提醒消費者在購買含NMN成分産品時(shí),請(qǐng)認真、仔細閱讀電(diàn)商網站(zhàn)上(shàng)風險告知書(shū)內(nèi)容,關注原産地信息,結合自身風險承擔能力做(zuò)出是否購買判斷。
此外去年,海關總署部署開(kāi)展跨境電(diàn)商網購保稅進口食品“健安2023”專項行(xíng)動,首次将保健食品列為(wèi)風險監測類,對跨境電(diàn)商進口保健食品開(kāi)展監測。此專項行(xíng)動中也發現含β-煙酰胺單核苷酸(俗稱“不老藥”,NMN)類等保健食品中有(yǒu)有(yǒu)效成分虛假标示等問題。
06
關于開(kāi)展嚴厲打擊肉類産品違法犯罪專項整治行(xíng)動的通(tōng)知
針對3·15晚會(huì)播出的個(gè)别企業使用槽頭肉制(zhì)作(zuò)預制(zhì)菜的情況,當地的監督檢查執法行(xíng)動正在展開(kāi)。針對監管中發現的個(gè)别不法企業的違法犯罪行(xíng)為(wèi),國務院食安辦将會(huì)同公安部、農業農村部、市場(chǎng)監管總局等部門(mén),在全國範圍內(nèi)開(kāi)展為(wèi)期8個(gè)月的嚴厲查處使用“瘦肉精”等違禁藥品、生(shēng)産假冒牛(羊、驢)肉制(zhì)品等違法行(xíng)為(wèi)專項整治行(xíng)動,保障肉類産品質量安全。

來(lái)源:中食安信
中食安信是一家(jiā)專業服務于食品行(xíng)業的法規咨詢機構,緻力于為(wèi)全球食品行(xíng)業客戶提供食品标準法規咨詢、食品相關報批注冊、食品合規管理(lǐ)系統、食品行(xíng)業信息服務等全方位、全流程的食品合規管理(lǐ)咨詢服務。
咨詢電(diàn)話(huà):010-51301566










 京公網安備11010502045875
京公網安備11010502045875