食品科學技(jì)術(shù)及工業的發展和(hé)貿易全球化促進了中國市場(chǎng)上(shàng)食品來(lái)源的多(duō)樣性。其中較為(wèi)明(míng)顯的趨勢便是食品及原料的供應日益全球化,食品原料的種類和(hé)來(lái)源也随之不斷擴大(dà),一些(xiē)在中國沒有(yǒu)傳統食用習慣的食品原料也逐漸進入消費者的視(shì)野。為(wèi)了規範食品原料的開(kāi)發和(hé)應用,保障食品安全,這些(xiē)原料在進入市場(chǎng)銷售前必須要進行(xíng)新食品原料的申報與評估,經國家(jiā)衛生(shēng)健康委員會(huì)(下文簡稱為(wèi)衛健委)批準,才可(kě)進行(xíng)銷售。為(wèi)促進各企業對新食品原料的了解,避免出現食品合規性問題,此簡介對中國新食品原料管理(lǐ)制(zhì)度進行(xíng)了介紹。
一、 新食品原料介紹
新食品原料這一名詞的前身為(wèi)新資源食品,最初來(lái)源于1983年中國頒布的《食品衛生(shēng)法(試行(xíng))》其中第二十二條規定(“利用新資源生(shēng)産的食品必須經衛生(shēng)部門(mén)審批”),由此初步确定了新資源食品的基本管理(lǐ)制(zhì)度。此後,2009年頒布實施的《食品安全法》第四十四條中則使用了“新的食品原料”這一表述。2013年,随着《新食品原料安全性審查管理(lǐ)辦法》的頒布實施,“新資源食品”正式更名為(wèi)“新食品原料”并延續使用至今。目前現行(xíng)的《新食品原料安全性審查管理(lǐ)辦法》已實施将近13年之久,預測未來(lái)新食品原料相關的法規也将進行(xíng)整改修訂,進一步明(míng)确細化管理(lǐ)制(zhì)度及法規內(nèi)容,查缺補漏。
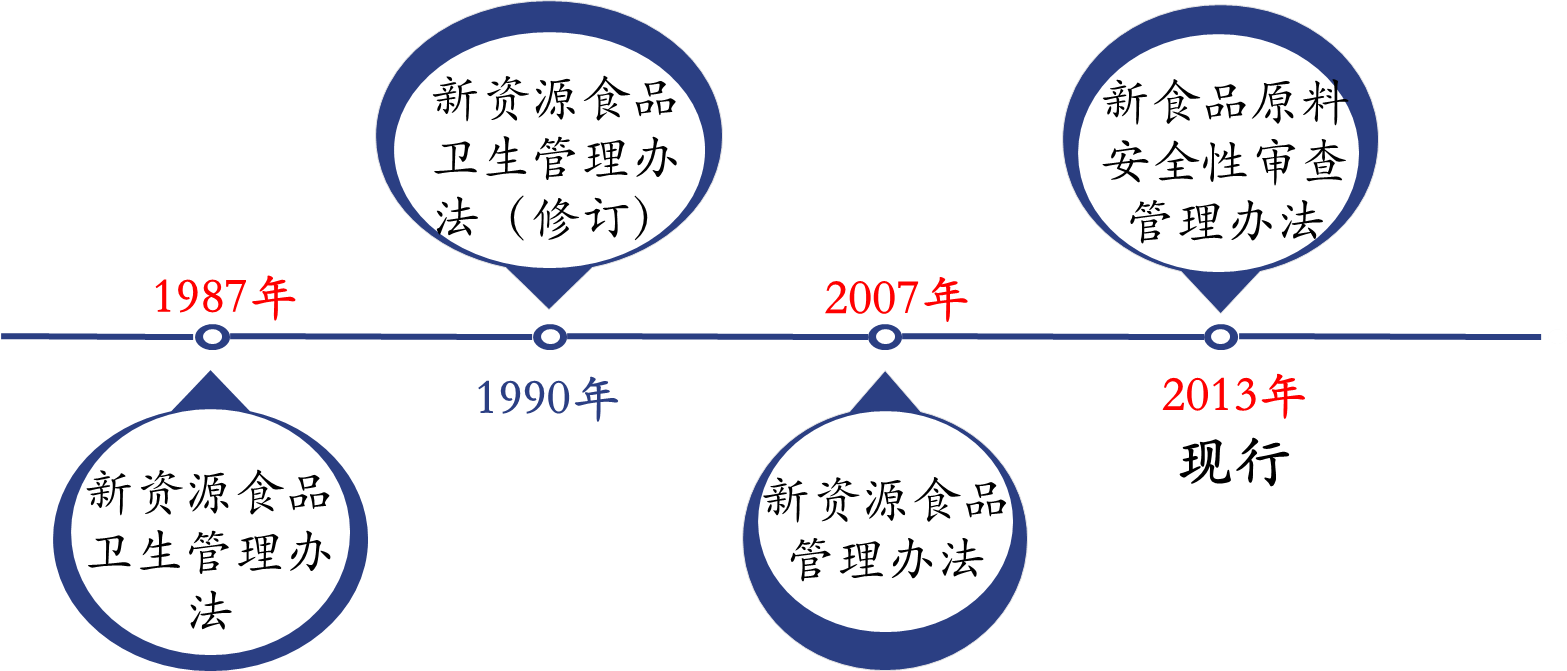
來(lái)源:中食安信
圖1:新食品原料法規發展進程
自1987年至2007年,食品終産品和(hé)食品原料均可(kě)以按照新資源食品劃分,随着管理(lǐ)規定的更新,自2007年12月起,此類規定的管理(lǐ)對象被限定在食品原料方面,此外,對此類原料的定義和(hé)範圍也逐漸明(míng)确并細化。同時(shí),随着相關管理(lǐ)規定的完善,現行(xíng)有(yǒu)效的《新食品原料安全性審查管理(lǐ)辦法》還(hái)明(míng)确了不符合申報要求的4種非新食品原料:1. 不具有(yǒu)食品原料特性的物質;2. 已列入GB 2760和(hé)GB 14880的物質(即食品添加劑和(hé)營養強化劑);3. 國家(jiā)衛健委已作(zuò)出不予行(xíng)政許可(kě)的物質;4. 其他不符合有(yǒu)關法律法規規定的物質。
就批準情況來(lái)看,自2008年至2019年,公告批準的新食品原料總數(shù)為(wèi)130個(gè)(具體(tǐ)情況見圖2,具體(tǐ)批準原料列表見表1)。
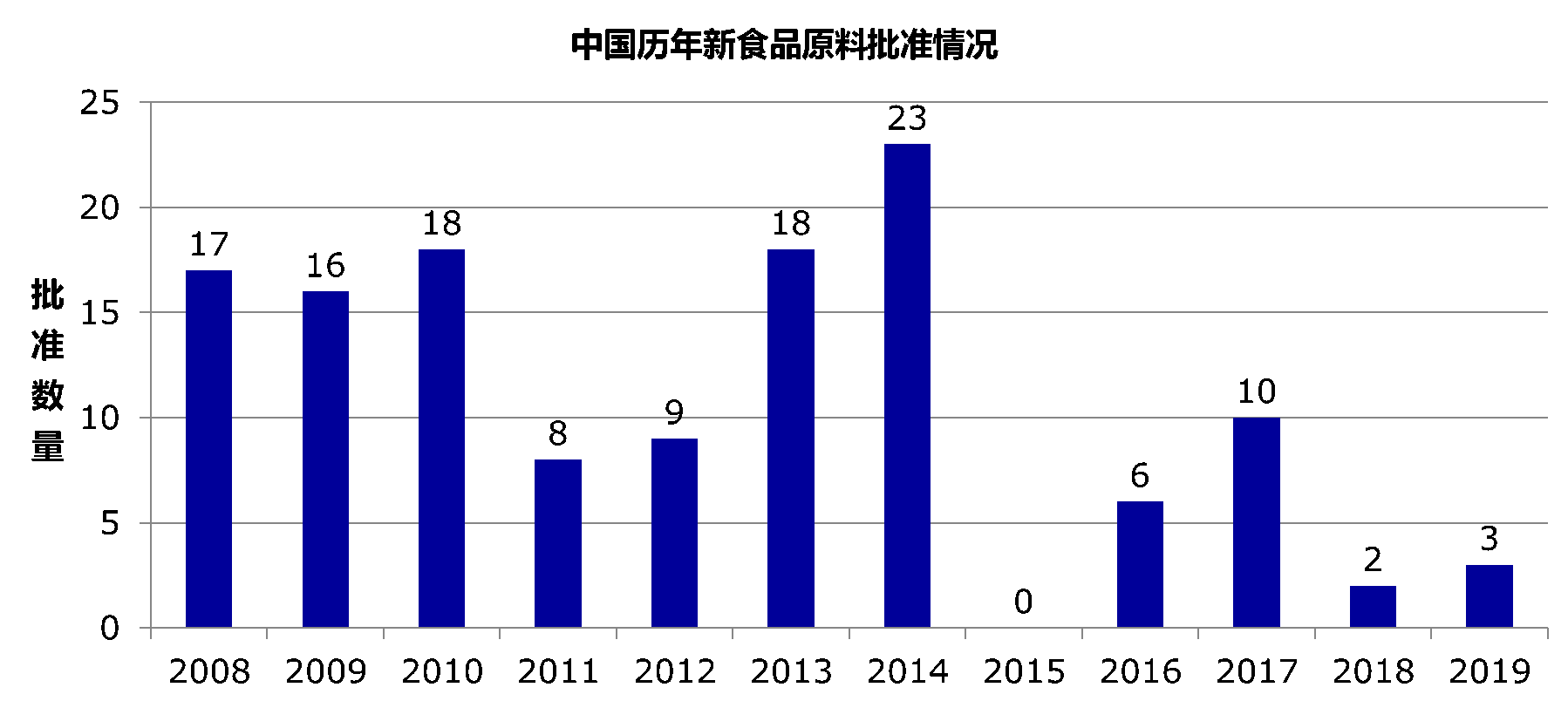
來(lái)源:中食安信
圖2:中國曆年新食品原料批準情況
表1:中國曆年批準的新食品原料列表
年份 | 新食品原料名稱 |
2008 | 嗜酸乳杆菌(菌株号:DSM13241)、透明(míng)質酸鈉、葉黃素酯、L-阿拉伯糖、短(duǎn)梗五加、庫拉索蘆荟凝膠、低(dī)聚半乳糖、副幹酪乳杆菌(菌株号:GM080、GMNL-33)、嗜酸乳杆菌(菌株号:R0052)、鼠李糖乳杆菌(菌株号:R0011)、水(shuǐ)解蛋黃粉、異麥芽酮糖醇、植物乳杆菌(菌株号:299v)、植物乳杆菌(菌株号:CGMCC NO.1258)、植物甾烷醇酯、低(dī)聚木糖、珠肽粉 |
2009 | 蛹蟲草、菊粉、多(duō)聚果糖、γ-氨基丁酸、初乳堿性蛋白粉、共轭亞油酸、共轭亞油酸甘油酯、植物乳杆菌(菌株号:ST-Ⅲ)、杜仲籽油、茶葉籽油、鹽藻及提取物、魚油及提取物、甘油二酯油、地龍蛋白、乳礦物鹽、牛奶堿性蛋白 |
2010 | DHA藻油、棉子低(dī)聚糖、植物甾醇酯、植物甾醇、花(huā)生(shēng)四烯酸油脂、白子菜、禦米油、金花(huā)茶、顯脈旋覆花(huā)(小(xiǎo)黑(hēi)藥)、諾麗(lì)果漿、酵母β-葡聚糖、雪蓮培養物、蔗糖聚酯、玉米低(dī)聚肽粉、磷脂酰絲氨酸、雨生(shēng)紅球藻、表沒食子兒茶素沒食子酸酯、費氏丙酸杆菌謝氏亞種 |
2011 | 翅果油、β-羟基-β-甲基丁酸、元寶楓籽油、牡丹籽油、瑪咖粉、乳酸乳球菌乳酸亞種、乳酸乳球菌乳脂亞種、乳酸乳球菌雙乙酰亞種 |
2012 | 蚌肉多(duō)糖、中長鏈脂肪酸、小(xiǎo)麥低(dī)聚肽、人(rén)參(人(rén)工種植)、蛋白核小(xiǎo)球藻、烏藥葉、辣木葉、蔗糖聚酯、腸膜明(míng)串珠菌腸膜亞種 |
2013 | 茶樹(shù)花(huā)、鹽地堿蓬籽油、美藤果油、鹽膚木果油、廣東蟲草子實體(tǐ)、阿薩伊果、茶藨子葉狀層菌發酵菌絲體(tǐ)、裸藻、1,6-二磷酸果糖三鈉、丹鳳牡丹花(huā)、狹基線紋香茶菜、長柄扁桃油、光皮梾木果油、青錢(qián)柳葉、低(dī)聚甘露糖、顯齒蛇葡萄葉、磷蝦油、馬克斯克魯維酵母 |
2014 | 殼寡糖、水(shuǐ)飛薊籽油、柳葉蠟梅、杜仲雄花(huā)、線葉金雀花(huā)、塔格糖、奇亞籽、圓苞車(chē)前子殼、羅伊氏乳杆菌(菌株号:DSM17938)、蛹蟲草、植物甾烷醇酯、茶葉茶氨酸、番茄籽油、枇杷葉、阿拉伯半乳聚糖、湖(hú)北海棠(茶海棠)葉、竹葉黃酮、燕麥β-葡聚糖、清酒乳杆菌、産丙酸丙酸杆菌、低(dī)聚木糖(調整)、乳酸片球菌、戊糖片球菌 |
2015 | 無 |
2016 | 肉葡萄球菌、發酵乳杆菌(菌株号:CECT5716)、短(duǎn)雙歧杆菌(菌株号:M-16V)、凝結芽孢杆菌、小(xiǎo)牛葡萄球菌、木糖葡萄球菌 |
2017 | 乳木果油、(3R,3'R)-二羟基-β-胡蘿蔔素、寶樂果粉、N-乙酰神經氨酸、順-15-二十四碳烯酸、西蘭花(huā)種子水(shuǐ)提物、米糠脂肪烷醇、γ-亞麻酸油脂(來(lái)源于刺孢小(xiǎo)克銀漢黴)、β-羟基-β-甲基丁酸鈣、木姜葉柯、 |
2018 | 黑(hēi)果腺肋花(huā)楸果、球狀念珠藻(葛仙米) |
2019 | 彎曲乳杆菌、明(míng)日葉、枇杷花(huā) |
二、新食品原料申報材料要求
如果企業使用的原料符合新食品原料的定義,則在使用前需将原料申報為(wèi)新食品原料。根據《新食品原料申報與受理(lǐ)規定》的要求,申請(qǐng)新食品原料所需的材料有(yǒu)以下內(nèi)容(具體(tǐ)細節要求需根據不同原料的種類而定):
(1)申請(qǐng)表
(2)新食品原料研制(zhì)報告
(3)安全性評估報告
a) 成分分析報告
b) 衛生(shēng)學檢驗報告(有(yǒu)資質要求)
c) 毒理(lǐ)學評價報告
(有(yǒu)資質要求,試驗項目根據國內(nèi)外使用情況而定,項目數(shù)波動範圍為(wèi)2~7項)
d) 微生(shēng)物耐藥性試驗和(hé)産毒能力試驗(有(yǒu)資質要求,僅針對微生(shēng)物)
e) 安全性評估意見
(需提供申報物質基本信息、成分分析、毒理(lǐ)學資料、人(rén)群資料、食用和(hé)使用情況和(hé)攝入量評估等信息給符合資質要求的機構撰寫)
(4)生(shēng)産工藝
(5)執行(xíng)的相關标準
(6)标簽及說明(míng)書(shū)
(7)國內(nèi)外研究利用情況和(hé)相關安全性評估資料
(8)申報委托書(shū)(委托代理(lǐ)申報時(shí)提供)
(9)有(yǒu)助于評審的其他資料
(10)未啓封最小(xiǎo)包裝的樣品1件或者原料30克
此外,申報物質為(wèi)進口的情況下,還(hái)需提供以下文件:
(11)進口新食品原料需提交的材料
a) 進口新食品原料出口國(地區(qū))相關部門(mén)或者機構出具的允許該産品在本國(地區(qū))生(shēng)産或者銷售的證明(míng)材料
b) 進口新食品原料生(shēng)産企業所在國(地區(qū))有(yǒu)關機構或者組織出具的對生(shēng)産企業審查或者認證的證明(míng)材料
三、新食品原料審批流程
新食品原料的具體(tǐ)審批流程可(kě)見圖3。
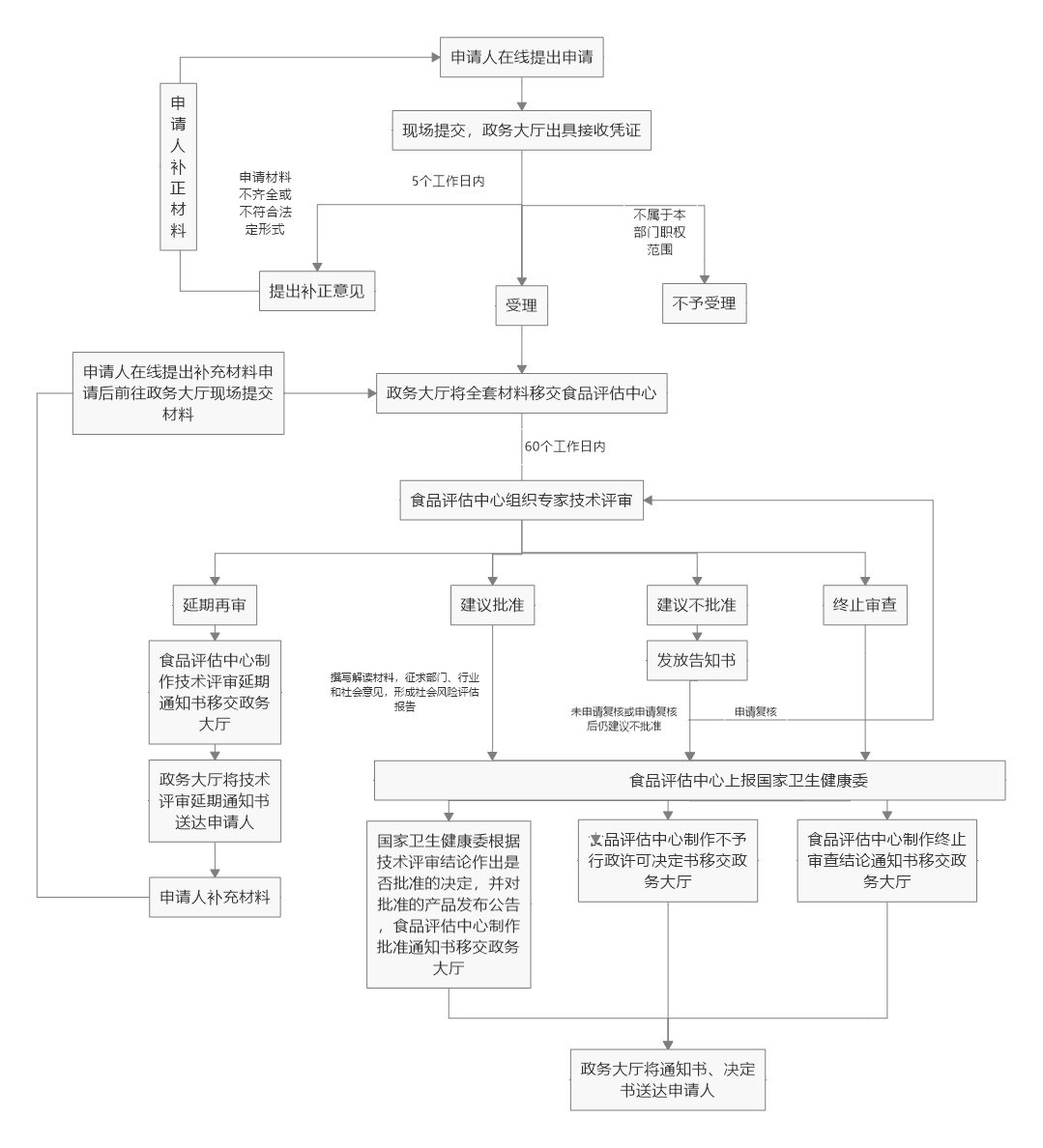
來(lái)源:參照衛健委官網
圖3:新食品原料審批行(xíng)政許可(kě)工作(zuò)流程圖
四、審評結論
由圖3可(kě)知,新食品原料的審查結論分為(wèi)4種情況,分别為(wèi)延期再審、建議批準、建議不批準和(hé)終止審查,對于這些(xiē)情況的具體(tǐ)說明(míng)如下:
延期再審
如果提交的申報材料有(yǒu)需要修改、補充的內(nèi)容,或是需要進一步進行(xíng)驗證性試驗或科學論證的情況,衛健委會(huì)出具“行(xíng)政許可(kě)技(jì)術(shù)評審延期通(tōng)知書(shū)”,申請(qǐng)人(rén)需根據通(tōng)知書(shū)內(nèi)容,補充提交缺少(shǎo)的申報材料,再進行(xíng)一次專家(jiā)審評。
建議批準
如果申報物質通(tōng)過專家(jiā)組織的審評且結論為(wèi)“建議批準”,衛生(shēng)健康會(huì)員會(huì)會(huì)面向社會(huì)征求意見,征求意見時(shí)間(jiān)為(wèi)30日。此後,衛健委會(huì)對征求的意見進行(xíng)研究,最後由衛健委出具“行(xíng)政許可(kě)審查結論通(tōng)知”。
建議不批準
如果申報的物質出現不符合新食品原料定義(比如不具有(yǒu)食品原料特性),或不符合應當有(yǒu)的營養要求,或安全性不能保證等情況,技(jì)術(shù)評審結論會(huì)為(wèi)“建議不批準”。衛健委會(huì)向申請(qǐng)人(rén)出具“行(xíng)政許可(kě)技(jì)術(shù)評審意見告知書(shū)”。如果申請(qǐng)人(rén)對此結論有(yǒu)異議,可(kě)在30日內(nèi)提出複核申請(qǐng),如複核後結論仍為(wèi)“建議不批準”或逾期未提出複核申請(qǐng)的,則衛健委會(huì)像申請(qǐng)人(rén)出具“不予行(xíng)政許可(kě)決定書(shū)”,并告知不予許可(kě)的理(lǐ)由。
需要注意的是,如果申報材料或樣品不真實也會(huì)造成“建議不批準”的情況。此外,按照上(shàng)文非新食品原料的定義,不予行(xíng)政許可(kě)的物質不能再次申報新食品原料。
終止審查
如果申報的物質為(wèi)普通(tōng)食品原料,或與普通(tōng)食品原料或已批準的新食品原料實質等同,則衛健委會(huì)會(huì)向申請(qǐng)人(rén)出具“行(xíng)政許可(kě)終止審查通(tōng)知書(shū)”,并告知終止審查的理(lǐ)由。
實質等同一詞出自于2007年的《新資源食品管理(lǐ)辦法》,是指如某個(gè)新申報的食品原料與食品或者已公布的新食品原料在種屬、來(lái)源、生(shēng)物學特征、主要成分、食用部位、使用量、使用範圍和(hé)應用人(rén)群等方面相同,所采用工藝和(hé)質量要求基本一緻,可(kě)以視(shì)為(wèi)它們是同等安全的,具有(yǒu)實質等同性。
五、參考法規
《食品安全法》
《新資源食品管理(lǐ)辦法》
《新食品原料安全性審查管理(lǐ)辦法》
《新食品原料申報與受理(lǐ)規定》
《新食品原料安全性審查規程》
新食品原料申報可(kě)行(xíng)性評估及新食品原料的全程代理(lǐ)審報服務
新食品原料的申報過程較為(wèi)複雜,審批周期相對較長,注冊過程中需提供的申報材料和(hé)補正材料等均有(yǒu)嚴格的要求,對企業來(lái)說需要有(yǒu)專門(mén)的團隊或人(rén)員配合,企業需提前做(zuò)好充分準備。中食安信可(kě)提供新食品原料申報可(kě)行(xíng)性評估服務,以及新食品原料的全程代理(lǐ)審報服務,提高(gāo)企業申報效率,降低(dī)人(rén)力、資金成本。有(yǒu)任何問題歡迎随時(shí)聯系我們(010-51301566)。










 京公網安備11010502045875
京公網安備11010502045875