八月份,各部委陸續發布了一批重要的法規标準,如國家(jiā)市場(chǎng)監管總局對食品經營許可(kě)、網絡直播帶貨等管理(lǐ)進公開(kāi)征求意見,同時(shí)還(hái)就輔酶Q10等五種保健食品原料目錄原料及凝膠糖果和(hé)粉劑等兩種備案劑型向社會(huì)公衆征求意見;國家(jiā)衛生(shēng)健康委員會(huì)新批準了21種“三新食品”,其中包括5種食品添加劑新品種,同時(shí),國家(jiā)衛健委對預包裝食品營養标簽通(tōng)則等16項食品安全國家(jiā)标準征求意見稿向社會(huì)公衆征求意見;因為(wèi)疫情的影(yǐng)響,海關總署就進口厄瓜多(duō)爾冷凍南美白蝦檢驗等事宜發布了相關公告……等等。為(wèi)了更好的幫助企業了解法規,中食安信對2020年8月發布的重點法規、标準以及征求意見稿進行(xíng)了解讀,同時(shí)對本月發布的食品相關法規标準等進行(xíng)了彙總,供大(dà)家(jiā)參考。
1、《市場(chǎng)監管總局關于加強網絡直播營銷活動監管的指導意見(征求意見稿)》
2020年7月29日,國家(jiā)市場(chǎng)監督管理(lǐ)總局發布了《市場(chǎng)監管總局關于加強網絡直播營銷活動監管的指導意見(征求意見稿)》(以下簡稱《征求意見稿》),并從即日起至8月28日向社會(huì)各界征求意見。這是我國首次将監管網絡直播營銷活動上(shàng)升至法制(zhì)層面。
該《征求意見稿》的主要內(nèi)容及影(yǐng)響包括以下幾點:
1) 明(míng)确網絡平台經營者、商品經營者及網絡主播的法律責任,應履行(xíng)《電(diàn)子商務法》規定相應的責任和(hé)義務,對網絡直播營銷活動進行(xíng)宣傳和(hé)推廣的,或直播內(nèi)容構成商業廣告的,還(hái)需遵守《廣告法》的相關規定;
2) 要求對營銷商品建立并執行(xíng)進貨檢查驗收制(zhì)度。指明(míng)限制(zhì)範圍,禁止生(shēng)産銷售的商品和(hé)煙草以及特定全營養配方食品不得(de)通(tōng)過網絡直播銷售,并且嚴格規範保健食品等特殊食品的網絡直播營銷行(xíng)為(wèi);
3) 明(míng)确網絡直播營銷違法行(xíng)為(wèi)處罰及處罰依據。
該《征求意見稿》明(míng)确了網絡營銷活動中出現的網絡平台責任落實不到位、商品經營者售賣假冒僞劣商品、網絡主播虛假宣傳等法律責任。《征求意見稿》若正式落地,直播營銷內(nèi)容基本等同于商業廣告,相關內(nèi)容依照《廣告法》等相關法律法規進行(xíng)審核約束。目前該《征求意見稿》仍處于征求意見階段,企業可(kě)根據實際情況及時(shí)反饋意見将法規進行(xíng)完善。
詳細解讀內(nèi)容請(qǐng)點擊:解讀《市場(chǎng)監管總局關于加強網絡直播營銷活動監管的指導意見(征求意見稿)》
2、備案制(zhì)保健食品迎來(lái)利好
2020年8月12日,市場(chǎng)監管總局發布了關于公開(kāi)征求輔酶Q10等五種保健食品原料目錄備案産品技(jì)術(shù)要求(征求意見稿)意見的公告,并對相關配套文件進行(xíng)征求意見。2019年3月,輔酶Q10、魚油、破壁靈芝孢子粉、螺旋藻和(hé)褪黑(hēi)素五種物質原料目錄已向社會(huì)公衆征求意見。經收集彙總反饋意見後,總局陸續開(kāi)展後續備案配套文件制(zhì)定工作(zuò),最終形成了五種原料可(kě)以備案的配套文件。此次征求意見截止至2020年9月12日。
該征求意見針對輔酶Q10等五種原料分别建立了體(tǐ)現保健食品原料特點的技(jì)術(shù)要求;采納了破壁靈芝孢子粉的粉劑劑型的建議,涉及劑型包括片劑、顆粒劑、硬膠囊、軟膠囊和(hé)粉劑;确定了五種備案産品的可(kě)用輔料名單;分别細化各原料各劑型的産品技(jì)術(shù)指标。
另外,2020年8月28日,市場(chǎng)監管局還(hái)發布了關于公開(kāi)征求将凝膠糖果、粉劑納入保健食品備案劑型意見的公告,制(zhì)定了凝膠糖果和(hé)粉劑備案的技(jì)術(shù)要求,并配套修訂《保健食品備案可(kě)用輔料及其适用規定(2020年版)(征求意見稿)》和(hé)《保健食品備案産品劑型及主要生(shēng)産工藝(2020年版)(征求意見稿)》。征求意見截止時(shí)間(jiān)為(wèi)2020年9月28日。
此次征求意見計(jì)劃将凝膠糖果、粉劑兩種劑型納入備案制(zhì)保健食品劑型,對凝膠糖果及粉劑的定義、産品說明(míng)書(shū)相關內(nèi)容、産品技(jì)術(shù)要求有(yǒu)關內(nèi)容和(hé)産品名稱進行(xíng)了相關規定,進一步擴大(dà)備案産品可(kě)用食品形态。
目前,這兩個(gè)征求意見稿仍處于征求意見階段,企業可(kě)根據實際情況及時(shí)反饋意見,說明(míng)企業實際存在的情況及案例,以期法規能夠更加完善,符合食品行(xíng)業的現狀及需求。
3、多(duō)項食品安全國家(jiā)标準公開(kāi)征求意見
2020年8月31日,國家(jiā)衛生(shēng)健康委員會(huì)發布了關于征求食品中污染物限量等16項食品安全國家(jiā)标準(征求意見稿)意見的函,即日起向社會(huì)公開(kāi)征求意見,截止時(shí)間(jiān)為(wèi)2020年10月20日。此次征求意見的16項食品安全國家(jiā)标準中,備受關注的标準包括以下幾項:
1)《食品安全國家(jiā)标準 預包裝食品營養标簽通(tōng)則》
主要修訂內(nèi)容有(yǒu):預包裝食品營養标簽強制(zhì)性标示內(nèi)容由‘1+4’改為(wèi)‘1+6’,即能量、蛋白質、飽和(hé)脂肪(或飽和(hé)脂肪酸)、碳水(shuǐ)化合物、糖和(hé)鈉,同時(shí)将以每100g和(hé)(或)每100mL可(kě)食部中的具體(tǐ)數(shù)值标示能量和(hé)營養成分調整為(wèi)強制(zhì)內(nèi)容,營養标簽格式也作(zuò)了相應的調整。增加了用“份”表達時(shí)的标示要求,并提供了食品份量參考值。明(míng)确了标示值的獲得(de)途徑。此外,對部分營養素的名稱、表達單位、聲稱等,以及營養标簽豁免範圍也進行(xíng)了修訂和(hé)調整。
2) 《食品安全國家(jiā)标準 調制(zhì)乳》
因考慮到其他奶畜類乳,因此将定義改為(wèi)“生(shēng)乳和(hé)/或複原乳為(wèi)主要原料”,增加複原乳定義。修改了标識要求,規定“複原乳”或“複原奶”與産品名稱應标識在包裝容器(qì)的同一展示版面。同時(shí),産品的技(jì)術(shù)要求和(hé)檢驗方法等也進行(xíng)了相應的修改。
3) 《食品安全國家(jiā)标準 再制(zhì)幹酪和(hé)幹酪制(zhì)品》
此次征求意見根據行(xíng)業市場(chǎng)情況,修改了“再制(zhì)幹酪”原輔料及工藝制(zhì)品的表述,并調整了其幹酪使用比例要求,新增對粉狀産品的說明(míng)。此外,新增了“幹酪制(zhì)品”的定義。同時(shí),産品技(jì)術(shù)要求也進行(xíng)了相應的調整、增加。明(míng)确了産品标識要求,需标識幹酪使用比例。
4) 《食品安全國家(jiā)标準 飲料》
細化了産品分類,明(míng)确了無醇啤酒不屬于飲料,并在此基礎上(shàng)修改了産品的技(jì)術(shù)要求,其中,值得(de)注意的是固體(tǐ)飲料的菌落總數(shù)從1000CFU/g改為(wèi)了10000CFU/g。在标簽标識方面,對于添加乳酸菌的活菌型産品,應在其标簽上(shàng)标識乳酸菌的含量。
目前,16項标準仍處于征求意見階段,企業可(kě)根據實際情況及時(shí)反饋意見,說明(míng)企業實際存在的情況及案例,以期标準能夠更加完善,符合食品行(xíng)業的現狀及需求。
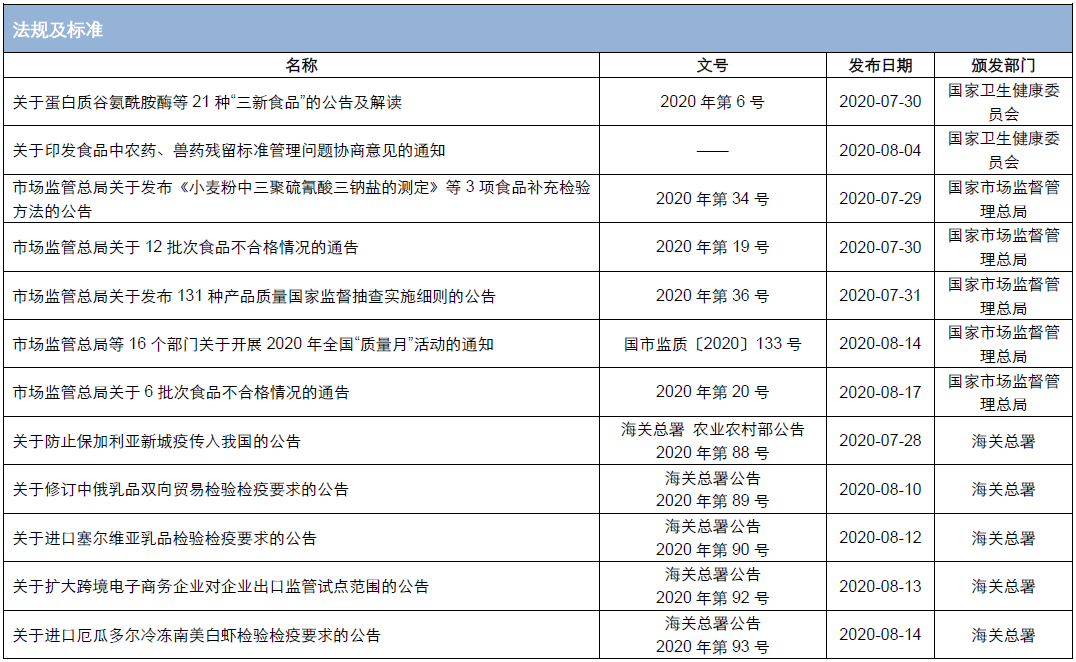
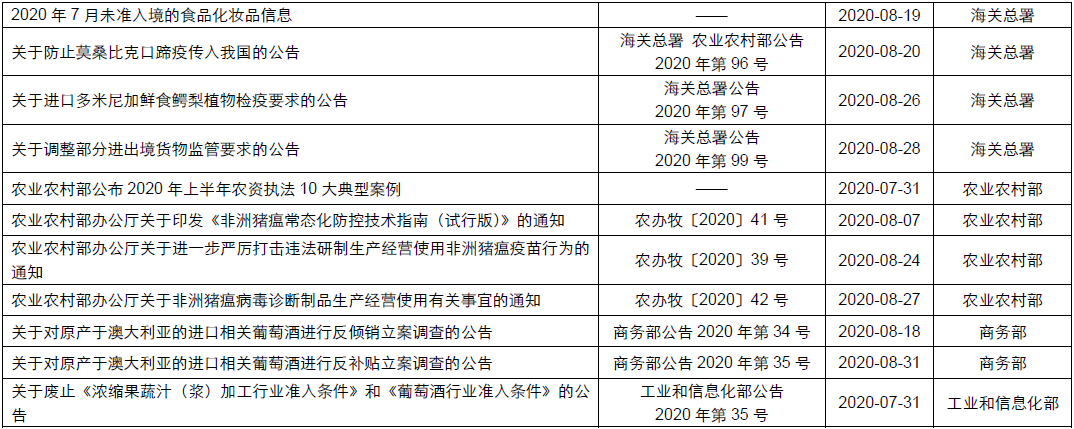
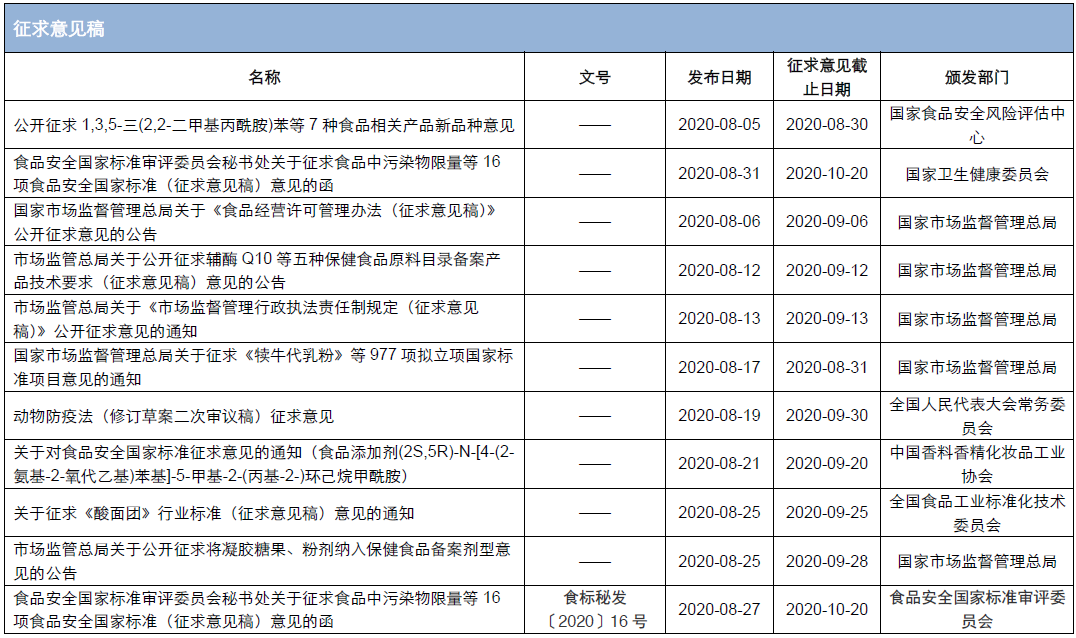
附件:2020年8月發布的具體(tǐ)法規、标準及征求意見稿詳見附件










 京公網安備11010502045875
京公網安備11010502045875