我國新食品原料經過多(duō)年發展,相應配套的法規标準已趨于完善。企業在生(shēng)産加工使用新食品原料時(shí),常常會(huì)忽略相關的一些(xiē)配套要求。随着越來(lái)越多(duō)的新食品原料通(tōng)過審批,為(wèi)企業合規安全的使用新食品原料,中食安信整理(lǐ)了部分注意事項,以供參考。
1.《關于“三新食品”目錄及适用的食品安全标準的公告》更新了食品安全指标要求
我國管理(lǐ)新食品原料的法規自1987年的《食品新資源衛生(shēng)管理(lǐ)辦法》到2013年《新食品原料安全性審查管理(lǐ)辦法》已經曆多(duō)次變革,其名稱也由“新資源食品”更名為(wèi)現今的“新食品原料”。部分此前公告的“新資源食品”或“新食品原料”的食品安全指标或不滿足最新《食品安全法》及實施條例的管理(lǐ)要求,因此2023年5月國家(jiā)衛生(shēng)健康委發布《關于“三新食品”目錄及适用的食品安全标準的公告》(2023年 第4号),對原衛生(shēng)部2009年第3号公告至國家(jiā)衛生(shēng)健康委2021年第9号公告的新食品原料(菌種除外)的98個(gè)新食品原料品種的食品安全指标進行(xíng)更新,包括過氧化值、真菌毒素、污染物和(hé)微生(shēng)物限量。《公告》要求在“三新食品”的監管、生(shēng)産和(hé)使用中應按照要求執行(xíng)該公告的相關标準,同時(shí)給予了18個(gè)月過渡期。參考以上(shàng)變動,中食安信建議企業可(kě)提前與原料供應商溝通(tōng),可(kě)在18個(gè)月過渡期落地前按照新的要求查驗原料。
2.兼顧《終止審查目錄》中的相應審查結果
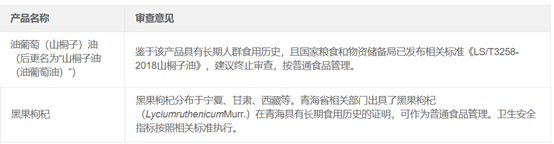
申請(qǐng)新食品原料除了得(de)到公告批準的形式之外,還(hái)有(yǒu)可(kě)能得(de)到的是“終止審查”的技(jì)術(shù)評審結論,其中“(一)經審核為(wèi)普通(tōng)食品或與普通(tōng)食品具有(yǒu)實質等同的;(二)與已公告的新食品原料具有(yǒu)實質等同的”的結果也可(kě)以作(zuò)為(wèi)食品原料使用依據。如“油葡萄油”、“黑(hēi)果枸杞”等已在終止審查結論中明(míng)确按照普通(tōng)食品管理(lǐ)。
3.注意新食品原料批準公告中的使用範圍
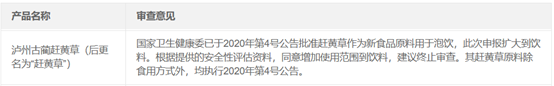
部分新食品原料公告中,除了注明(míng)“不适宜人(rén)群”、“安全指标”的要求外,會(huì)對食用方式進行(xíng)限制(zhì)。如《關于瑞士乳杆菌R0052等53種“三新食品”的公告》(2020年 第4号)批準的趕黃草,限定推薦食用量“≤8 克/天”,食用方式限定為(wèi)“泡飲”。因此将其用于開(kāi)發産品時(shí),注意不應将其作(zuò)為(wèi)直接食用的原料使用。

同時(shí),如第2條所述,兼顧《終止審查目錄》中的相應審查結果,趕黃草結合最新的審查結果,其使用範圍擴大(dà)到飲料中。企業研發時(shí)結合公告的同時(shí)也可(kě)以及時(shí)參考終止審查的結果。
4.标簽标示不可(kě)忽略新食品原料批準公告中要求
根據《新食品原料安全性審查管理(lǐ)辦法》第二十條,“食品中含有(yǒu)新食品原料的,其産品标簽标識應當符合國家(jiā)法律、法規、食品安全标準和(hé)國家(jiā)衛生(shēng)計(jì)生(shēng)委公告要求。”在使用新食品原料時(shí),要注意标簽應強制(zhì)标注相應內(nèi)容。如産品使用了透明(míng)質酸鈉時(shí),産品标簽應标注“嬰幼兒、孕婦及哺乳期婦女不宜食用,推薦食用量≤200 毫克/天”。

除了有(yǒu)明(míng)确要求标明(míng)使用範圍和(hé)限量的情況外,使用類似“菊粉”有(yǒu)食用限量但(dàn)無強制(zhì)規定的原料時(shí),建議參考《衛生(shēng)部等6部局關于含庫拉索蘆荟凝膠食品标識規定的公告》(2009年 第1号公告)“企業應在企業标準中對添加庫拉索蘆荟凝膠的食品的每日食用量作(zuò)出規定。若無法确保消費者蘆荟日攝入量在安全範圍內(nèi),應在包裝上(shàng)标注每日食用量警示語。”在終産品标簽寫明(míng)産品的每日食用量,以告知消費者,同時(shí)也是對于企業自身的保護。
以上(shàng)為(wèi)使用新食品原料時(shí)遇到的常見問題,另外中食安信将根據衛生(shēng)健康委員會(huì)定期發布“三新食品”的申報審批情況,希望對企業了解使用新食品原料有(yǒu)所幫助。
 京公網安備11010502045875
京公網安備11010502045875